

癌细胞有一个致命时弊,它们增殖太快,快到会把我方并吞在有毒的活性氧中。
问题是,癌细胞知说念这少量,是以它们会主动压制约略触发自我撤废的分子通路。以前十多年,科学家们一直试图找到一种要领,绕过这说念防地,免强癌细胞走向失掉。当今,这个糟蹋口终于出现了。
发表于顶级期刊《细胞》的最新探究娇傲,哥伦比亚大学赫伯特·欧文空洞癌症中心的探究团队,历时十年,终于破解了一种名为“铁失掉"的细胞失掉式样的自然触发机制,并找到了一个极具临床后劲的药物靶点。
铁失掉:一种被卡住的抗癌用具
铁失掉(ferroptosis)是2012年才被负责定名的细胞失掉式样,机制上与凋一火、坏死等经典失掉模式不止天渊。它依赖铁离子参与,通过细胞内脂质过氧化反应积攒到临界点,激勉法子性细胞崩解。
从表面上讲,铁失掉是凑合癌细胞的理思兵器。癌细胞因高速增殖而自然积攒大批活性氧(ROS),本应更容易被推向铁失掉的边际。问题是,执行室里能作念到这少量,主要靠化学妙技,而那些化学物成本人毒性太强,根柢不得看成念成药物。
更难办的是,此前探究发现的铁失掉中枢调控卵白GPX4,是细胞生计的必需品。让GPX4失去活性,动物胜利失掉,这意味着任何针对GPX4的药物,毒性齐可能难以收受。
通盘规模因此堕入了一种疾苦的僵局:知说念铁失掉灵验,却找不到安全可行的模式来触发它。
十年跟踪,从p53到圆善通路
这项探究的首先,不错回顾到2015年。
其时,论文资深作家魏顾率领团队发现,经典肿瘤阻难基因p53是铁失掉指引通路的要津参与者。但p53仅仅进口,通路上其他的分子是什么,其时完全不了了。
“当咱们发表那篇论文时,咱们就说必须找到原生信号,"魏顾回忆说念,"但最终花了十年,咱们才找到那条通路。"
{jz:field.toptypename/}拖了这样久,一个进犯原因是缺少印迹。现存文件简直一说念围绕化学指引的铁失掉通路伸开,自然触发机制在那边,莫得东说念主知说念从那边启动找。
探究团队决定接纳最暴力也最系统的要领:全基因组CRISPR筛查。
他们用CRISPR-Cas9基因剪辑时期,在培养的癌细胞中逐个敲除基因组里的每一个基因,然后不雅察哪些细胞失去了在高活性氧环境下发生铁失掉的材干。这额外于在一栋特别万个房间的大楼里,M6体育app官网逐间关灯,看哪间灯灭了之后整栋楼就暗了。
筛查成果指向了一个此前从未与铁失掉明确关连的基因:GPX1。
GPX1:精确打击癌细胞的新靶点
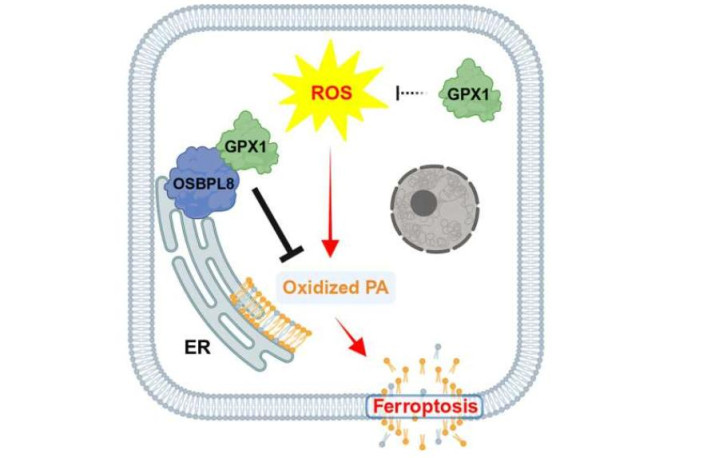
从GPX1启航,探究东说念主员向外彭胀,逐渐拼出了自然铁失掉通路的圆善图谱。
这是一个攀附运作的卵白质与脂质系统,负责感知细胞内活性氧的浓度并作念出反应。当活性氧积攒到危急水平,细胞濒临两个遴荐:要么启动诞守望制落拓毁伤,要么在无法诞生地触发法子性自毁,也便是铁失掉,以凝视受损细胞危害通盘机体。
GPX1在这套系统中上演的变装,与此前被视为“不行碰"的GPX4不止天渊。
GPX4对扫数细胞的生计齐不行或缺,失去它便是绝路一条。但GPX1是可替代的,至少在活性氧水公说念常的情况下如斯。探究发现,GPX1基因被敲除的动物约略时时发育滋长,莫得彰着额外。
这个发现兴味要紧。它意味着,在时时组织中,GPX1的缺失是不错被耐受的,但关于活性氧水平远高于时时细胞的癌细胞而言,GPX1是保管生计的所有依赖。
“癌细胞增殖速度极高,产生的活性氧水平远超时时细胞,"魏顾解说说念,“时时组织不错容忍GPX1的缺失,但癌细胞所有依赖GPX1来保管生计。"
这恰是一个理思药物靶点的特征:打击癌细胞,放落后时细胞。
从发现到药物,也曾在路上
探究团队并莫得停留在机制发现层面。
“咱们内容上正在制造GPX1阻难剂,"魏顾清楚,“由于它对时时细胞无效,只影响癌细胞或其他病理细胞,它们最终可能比现存疗法反作用更少。"
论文第一作家、顾执行室博士后夏章川示意,团队对GPX1作为新诊治政策靶点的后劲感到欢跃,利用边界不仅限于癌症,还包括以高活性氧为典型特征的神经退行性疾病,如亨廷顿病和帕金森病。
这一后劲彭胀是合理的。铁失掉通路的中枢逻辑是感知并反应氧化应激,而氧化应激在多种疾病的发病机制中齐上演着中枢变装。GPX1阻难剂若是约略遴荐性地在高活性氧环境中证据作用,表面上不错逾越多个疾病规模。
固然,从执行室的阻难剂到真是能用于临床的药物,还有漫长的路要走,包括动物执行、毒理学评估、临床教师的各个阶段。但主义也曾融会,靶点也曾找到,这在职何药物迷惑的故事里,齐是最难迈过的那一步。
十年,一个通路,一个靶点,和一扇从头翻开的门。

 备案号:
备案号: